انبساط و انقباض آب
انبساط و انقباض دو پدیدهی فیزیکی است که در اثر گرفتن و یا از دست دادن حرارت صورت میگیرد. ما در زندگی روزمره فراوان با این پدیده رو به رو میشویم و در صنعت نیز کاربردهای زیادی دارند. در این میان آب خاصیتی متفاوت در این پدیده نشان میدهد که علت آن را در این بخش بررسی میکنیم.
وقتی جسمی در اثر گرما جای بیشتری اشتغال می كند و بزرگتر می شود می گوییم منبسط شده است و هنگامی كه جسم در اثر سرما فضای كمتری اشغال می كند و كوچك تر می شود می گوییم منقبض شده است.
اگر بادكنكی را به دهانه یك بطری شیشه ایی خالی ببنیدم و بطری را درون ظرف آب داغ بگذاریم بادكنك باد می شود علت این پدیده انبساط هوای درون بادكنك بر اثر گرماست اگر بطری را درون مخلوط آب و یخ بگذاریم بادكنك دوباره چروكیده می شود.

گرما حجم مواد را تغییر می دهد. این پدیده را قانون انبساط و انقباض چنین بیان می كند:
ولی به طور کلی به شرح زیر است:

پدیده های بی شماری وجود دارند كه با اصل انبساط و انقباض قابل توضیح هستند از جمله:

از خودنویس پر از جوهر در روزهای گرم جوهر تراوش می كند.

سیم های برق را بین تیرها كمی شل می بندند.

گاهی در هوای گرم لاستیك اتومبیل ها می تركند.
انبساط و انقباض از دیدگاه نظریه مولكولی:
هنگامی كه ماده ایی گرم می شود جنبش و حركت مولكول های آن افزایش می یابد در نتیجه برخورد مولكول ها به یكدیگر بیشتر و فاصله بین مولكول ها زیادتر می شود. زیاد شدن فاصله مولكول ها از یكدیگر به افزایش حجم ماده (انبساط) منجر می شود. عكس این مطلب هم درست است یعنی وقتی ماده ایی سرد می شود جنبش مولكول ها كاهش و برخورد آن ها كم می شود در نتیجه مولكول ها به هم نزدیكتر و جسم كوچكتر (منقبض) می شود.
انبساط و انقباض آب،استثناء در این قانون
انبساط و انقباض آب با دیگر مایع ها متفاوت است و در آن استثناء وجود دارد. آب در دماهای بالاتر از 4 درجه ی سانتی گراد مانند دیگر مایع ها منبسط می شود اما در بین صفر درجه و تقریبا” چهار درجه ی سانتی گراد ، به جای منقبض شدن منبسط می شود. در دمای 4 درجه ی سانتی گراد ( 3/98 )، کم ترین حجم و آب در دماهای بالاتر از 4 درجه ی سانتی گراد مانند دیگر مایع ها منبسط می شود اما در بین صفر درجه و تقریبا” چهار درجه ی سانتی گراد، به جای منقبض شدن منبسط می شود.
بیشترین چگالی (جرم واحد حجم) را دارد و ماکزیمم چگالی آن 1 gr/cm³ است(9999750/)0, چگالی آب در دماهای دیگر از این مقدار کم تر است. به دلیل همین رفتار آب است که ابتدا سطح بالایی آن یخ می زند. اگر آب این چگالی ماکزیمم را نداشت، از پایین به بالا یخ می زد و مشکل آفرین می شد. در شکل زیر، نمودار حجم یک گرم آب و چگالی آب بر حسب دما کشیده شده است.
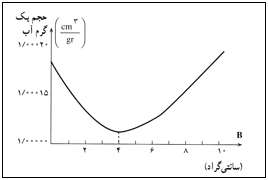
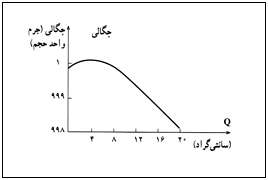
چرا آب استثناء است؟
هنگام انجماد آب مولكول های H2O در یك شش ضلعی باز قرار می گیرند هر اتم اكسیژن در بلور یخ به 4 هیدروژن وصل می شود كه با 2 اتم هیدروژن پیوند كووالانسی معمولی و با دوتای دیگر پیوند هیدروژنی تشكیل میدهد. بالا بودن نسبت فضای خالی در ساختمان یخ باعث كمتر شدن تراكم آن نسبت به آب می شود. افزایش حجم باعث كاهش چگالی آب می شود. سرد شدن آب تا زیر 4 درجه باعث كاهش تدریجی چگالی آب می شود و این نشان می دهد كه در نقطه انجماد آب انتقال از یك ساختمان مولكولی فشرده و بسته به یك ساختمان باز به طور ناگهانی صورت نمیگیرد بلكه به تدریج و در گستره دما انجام می شود.
با كاهش دما، مولكول های بیشتری به شكل ساختمان یخ میپیوندند و در دمای زیر 4 درجه تبدیل به ساختمان باز بر انقباض حاصل از سرد كردن غلبه كرده و با پایین آمدن دما به سمت 0 درجه آب منبسط می شود. انبساط آب به هنگام انجماد هم اثرات مفید و هم اثرات مضری دارد. انجماد آب در بافت های گیاهی و جانوری باعث تخریب دیواره سلولی در اثر انبساط می شود. اما همین فرایند انبساط در اثر یخ زدن آب در حفره های سنگ ها و صخره ها باعث شكستن سنگ ها شده و ایجاد خاك های حاصلخیز می كند.
مرکز یادگیری سایت تبیان - تهیه: مرتضی عرفانیان
تنظیم: مریم فروزان کیا

















